Τα πιο πρόσφατα κλινικά δεδομένα Φάσης ΙΙ της Novo Nordisk δείχνουν ότι ο διπλός αγωνιστής αμυλίνης GLP-1+αμυλίνης με ένα μόνο μόριο Amycretin έχει δείξει θετικά αποτελέσματα σε παχύσαρκους και διαβήτη τύπου 2 ασθενείς.


Βασική εισαγωγή Κινεζική ονομασία: πεπτίδιο τύπου γλυκαγόνης (GLP-1) και πολυπεπτίδιο αγωνιστή υποδοχέα αμυλίνης Αγγλική ονομασία: αμυκρετίνη/ζεναγκαμτίδη Αρ. εταιρείας: gt-l020/gt-m16083cas αρ.: 3005889-81-3 ακολουθία:H-His- {AIB} -Glu-Gly-PH-Ser-Glun-Glun-Glun-Glun-Glun-Glun-Glun-Gl-A)} - gly-gly-gly-gl-gl-day-gl-ped-gl-gl-dur-gl-gl-gl-gl-gl-gl-gl-gl-gl-glink-gl- Μοριακός τύπος: C343H50N94O116μοριακό βάρος: 7846,5753
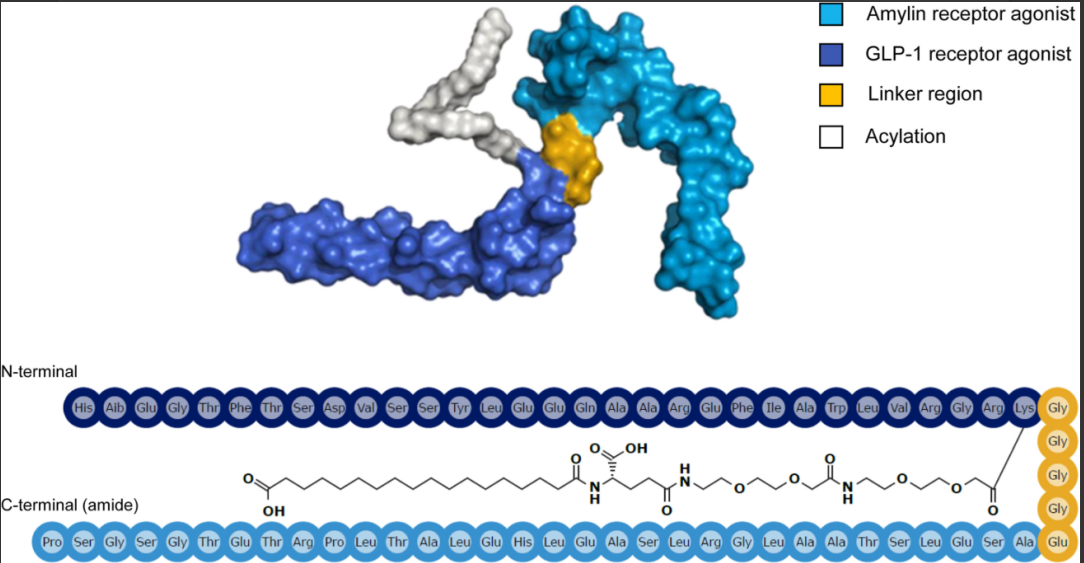
Τύπος χημικής δομής τουΕΝΑμυκρετίνη
Δυνατότητα απώλειας βάρους
Υποδόρια ένεση μία φορά την εβδομάδα, απώλεια βάρους έως και 14,5% σε 36 εβδομάδες και δεν παρατηρήθηκε οροπέδιο θεραπευτικής δράσης.
Σημαντικά σημεία από του στόματος σκευάσματα
Η καθημερινή από του στόματος χορήγηση αμυκρετίνης έδειξε επίσης καλά αποτελέσματα, με την HbA1c να μειώνεται έως και 1,5%.
Εάν η περαιτέρω επικύρωση είναι επιτυχής, αναμένεται να γίνει ένα άλλο από του στόματος φάρμακο GLP-1 που μπορεί να χρησιμοποιηθεί για απώλεια βάρους μετά από τον από του στόματος παράγοντα smeglutide, παρέχοντας πιο ευέλικτες επιλογές για τους ασθενείς.
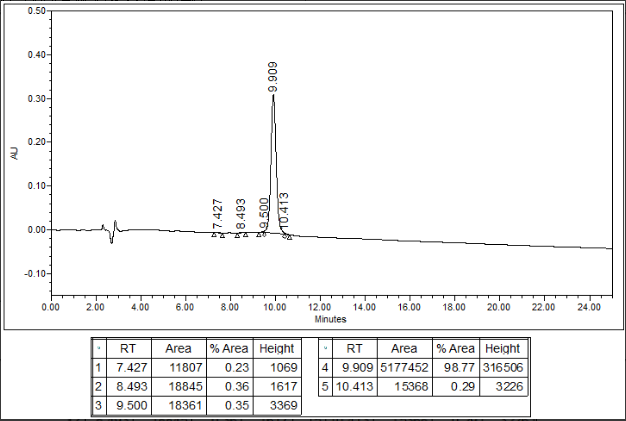
Αμυκρετίνη HPLC
Παρατήρηση ασφάλειας
Τα τρέχοντα κλινικά δεδομένα δείχνουν ότι η ασφάλεια είναι σύμφωνη με την υπάρχουσα θεραπεία με glp-1/αμυλίνη, κυρίως με ήπιες έως μέτριες γαστρεντερικές αντιδράσεις.
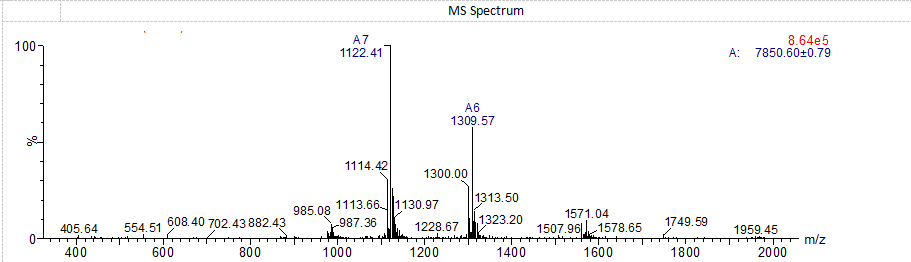
Αμυκρετίνη MS
Κλινική σημασία
Αυτή είναι η πρώτη συστηματική αξιολόγηση της αμυκρετίνης σε ασθενείς με σακχαρώδη διαβήτη τύπου 2. Τα αποτελέσματα δείχνουν ότι η επίδρασή του στην απώλεια βάρους είναι σημαντική και η δυνατότητα της από του στόματος + ένεσης ευελιξίας διπλού τρόπου λειτουργίας.
Εάν η κλινική επικύρωση παρακολούθησης είναι επιτυχής, αναμένεται να εισέλθει σε κλινικές δοκιμές φάσης 3.
Αποποίηση ευθύνης: Αυτό το άρθρο είναι μια μελέτη ανταλλαγής κλάδου. Τα πνευματικά δικαιώματα ανήκουν στον αρχικό δημιουργό. Εάν υπάρχει παράβαση, μπορείτε να επικοινωνήσετε για να τη διαγράψετε
Ώρα δημοσίευσης: 2025-12-01
