Τα πεπτίδια είναι μια κατηγορία ενώσεων που σχηματίζονται από τη σύνδεση πολλαπλών αμινοξέων μέσω πεπτιδικών δεσμών.Είναι πανταχού παρόντα στους ζωντανούς οργανισμούς.Μέχρι τώρα, δεκάδες χιλιάδες πεπτίδια έχουν βρεθεί σε ζωντανούς οργανισμούς.Τα πεπτίδια παίζουν σημαντικό ρόλο στη ρύθμιση των λειτουργικών δραστηριοτήτων διαφόρων συστημάτων, οργάνων, ιστών και κυττάρων και σε δραστηριότητες ζωής και χρησιμοποιούνται συχνά στη λειτουργική ανάλυση, στην έρευνα αντισωμάτων, στην ανάπτυξη φαρμάκων και σε άλλους τομείς.Με την ανάπτυξη της βιοτεχνολογίας και της τεχνολογίας σύνθεσης πεπτιδίων, όλο και περισσότερα πεπτιδικά φάρμακα έχουν αναπτυχθεί και εφαρμόζονται στην κλινική.
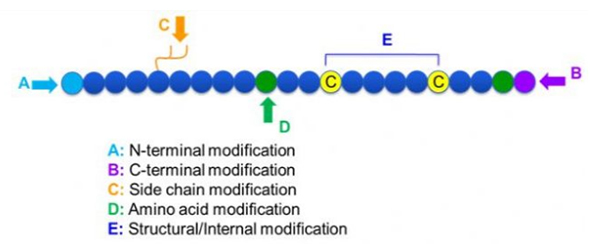
Υπάρχει μια μεγάλη ποικιλία από τροποποιήσεις πεπτιδίων, οι οποίες μπορούν απλά να χωριστούν σε μετατροποποίηση και τροποποίηση διεργασίας (χρησιμοποιώντας τροποποίηση αμινοξέος προερχόμενης), και τροποποίηση Ν-τερματικού, C-τερματική τροποποίηση, τροποποίηση πλευρικής αλυσίδας, τροποποίηση αμινοξέων, τροποποίηση σκελετού, κ.λπ., ανάλογα με τον τόπο τροποποίησης (Εικόνα 1).Ως σημαντικό μέσο για την αλλαγή της δομής της κύριας αλυσίδας ή των ομάδων πλευρικής αλυσίδας των πεπτιδικών αλυσίδων, η τροποποίηση πεπτιδίου μπορεί να αλλάξει αποτελεσματικά τις φυσικές και χημικές ιδιότητες των πεπτιδικών ενώσεων, να αυξήσει τη διαλυτότητα στο νερό, να παρατείνει τον χρόνο δράσης in vivo, να αλλάξει τη βιολογική κατανομή τους, να εξαλείψει την ανοσογονικότητα , μειώνουν τις τοξικές παρενέργειες, κ.λπ. Σε αυτή την εργασία, παρουσιάζονται αρκετές σημαντικές στρατηγικές τροποποίησης πεπτιδίων και τα χαρακτηριστικά τους.
1. Κυκλοποίηση
Τα κυκλικά πεπτίδια έχουν πολλές εφαρμογές στη βιοϊατρική και πολλά φυσικά πεπτίδια με βιολογική δράση είναι κυκλικά πεπτίδια.Επειδή τα κυκλικά πεπτίδια τείνουν να είναι πιο άκαμπτα από τα γραμμικά πεπτίδια, είναι εξαιρετικά ανθεκτικά στο πεπτικό σύστημα, μπορούν να επιβιώσουν στον πεπτικό σωλήνα και παρουσιάζουν ισχυρότερη συγγένεια με τους υποδοχείς στόχους.Η κυκλοποίηση είναι ο πιο άμεσος τρόπος για τη σύνθεση κυκλικών πεπτιδίων, ειδικά για πεπτίδια με μεγάλο δομικό σκελετό.Σύμφωνα με τη λειτουργία κυκλοποίησης, μπορεί να χωριστεί σε τύπο αλυσίδας πλευρικής αλυσίδας, τύπος τερματικού - πλευρικής αλυσίδας, τερματικός - τύπος τερματικού (τύπος από άκρο σε άκρο).
(1) πλευρική αλυσίδα σε πλευρική αλυσίδα
Ο πιο κοινός τύπος κυκλοποίησης πλευρικής αλυσίδας σε πλευρική αλυσίδα είναι η γεφύρωση δισουλφιδίου μεταξύ των υπολειμμάτων κυστεΐνης.Αυτή η κυκλοποίηση εισάγεται από ένα ζεύγος υπολειμμάτων κυστεΐνης που αποπροστατεύονται και στη συνέχεια οξειδώνονται για να σχηματίσουν δισουλφιδικούς δεσμούς.Η πολυκυκλική σύνθεση μπορεί να επιτευχθεί με επιλεκτική απομάκρυνση ομάδων προστασίας σουλφυδρυλίου.Η κυκλοποίηση μπορεί να γίνει είτε σε διαλύτη μετά τη διάσπαση είτε σε ρητίνη προδιάσπασης.Η κυκλοποίηση σε ρητίνες μπορεί να είναι λιγότερο αποτελεσματική από την κυκλοποίηση με διαλύτη επειδή τα πεπτίδια στις ρητίνες δεν σχηματίζουν εύκολα κυκλοποιημένες διαμορφώσεις.Ένας άλλος τύπος κυκλοποίησης πλευρικής αλυσίδας - πλευρικής αλυσίδας είναι ο σχηματισμός μιας δομής αμιδίου μεταξύ ενός υπολείμματος ασπαρτικού οξέος ή γλουταμινικού οξέος και του βασικού αμινοξέος, το οποίο απαιτεί ότι η ομάδα προστασίας πλευρικής αλυσίδας πρέπει να μπορεί να αφαιρεθεί επιλεκτικά από το πολυπεπτίδιο είτε στη ρητίνη ή μετά από διάσπαση.Ο τρίτος τύπος κυκλοποίησης πλευρικής αλυσίδας - πλευρικής αλυσίδας είναι ο σχηματισμός διφαινυλαιθέρων από τυροσίνη ή π-υδροξυφαινυλγλυκίνη.Αυτός ο τύπος κυκλοποίησης σε φυσικά προϊόντα βρίσκεται μόνο σε μικροβιακά προϊόντα και τα προϊόντα κυκλοποίησης έχουν συχνά πιθανή φαρμακευτική αξία.Η παρασκευή αυτών των ενώσεων απαιτεί μοναδικές συνθήκες αντίδρασης, επομένως δεν χρησιμοποιούνται συχνά στη σύνθεση συμβατικών πεπτιδίων.
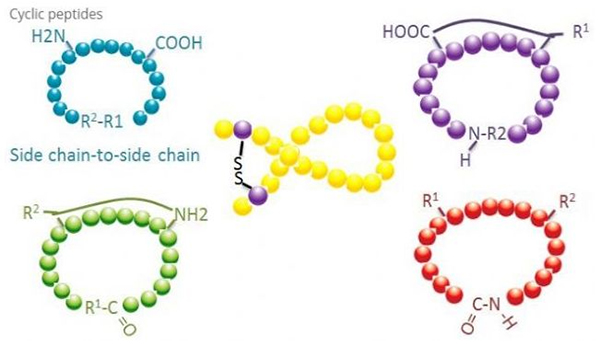
(2) τερματική προς πλευρική αλυσίδα
Η κυκλοποίηση της τελικής πλευρικής αλυσίδας συνήθως περιλαμβάνει το Ο-τελικό με την αμινομάδα της πλευρικής αλυσίδας λυσίνης ή ορνιθίνης ή το Ν-τελικό με την πλευρική αλυσίδα ασπαρτικού οξέος ή γλουταμικού οξέος.Άλλη κυκλοποίηση πολυπεπτιδίου γίνεται με σχηματισμό αιθερικών δεσμών μεταξύ του τερματικού C και των πλευρικών αλυσίδων σερίνης ή θρεονίνης.
(3) Τύπος τερματικού ή κεφαλής προς την ουρά
Τα πολυπεπτίδια αλυσίδας μπορούν είτε να ανακυκλωθούν σε έναν διαλύτη είτε να στερεωθούν σε μια ρητίνη με κυκλοποίηση πλευρικής αλυσίδας.Θα πρέπει να χρησιμοποιούνται χαμηλές συγκεντρώσεις πεπτιδίων στον συγκεντρωτισμό διαλύτη για να αποφευχθεί ο ολιγομερισμός των πεπτιδίων.Η απόδοση ενός πολυπεπτιδίου συνθετικού δακτυλίου από κεφαλή σε ουρά εξαρτάται από την αλληλουχία του πολυπεπτιδίου της αλυσίδας.Ως εκ τούτου, πριν από την παρασκευή κυκλικών πεπτιδίων σε μεγάλη κλίμακα, θα πρέπει πρώτα να δημιουργηθεί μια βιβλιοθήκη πιθανών πεπτιδίων μολύβδου με αλυσίδα, ακολουθούμενη από κυκλοποίηση για να βρεθεί η αλληλουχία με τα καλύτερα αποτελέσματα.
2. Ν-μεθυλίωση
Η Ν-μεθυλίωση εμφανίζεται αρχικά σε φυσικά πεπτίδια και εισάγεται στη σύνθεση πεπτιδίων για να αποτρέψει το σχηματισμό δεσμών υδρογόνου, καθιστώντας έτσι τα πεπτίδια πιο ανθεκτικά στη βιοαποδόμηση και την κάθαρση.Η σύνθεση πεπτιδίων χρησιμοποιώντας παράγωγα Ν-μεθυλιωμένων αμινοξέων είναι η πιο σημαντική μέθοδος.Επιπλέον, μπορεί επίσης να χρησιμοποιηθεί αντίδραση Mitsunobu των ενδιαμέσων πολυπεπτιδίου-ρητίνης Ν-(2-νιτροβενζολοσουλφονυλοχλωρίδιο) με μεθανόλη.Αυτή η μέθοδος έχει χρησιμοποιηθεί για την παρασκευή βιβλιοθηκών κυκλικών πεπτιδίων που περιέχουν Ν-μεθυλιωμένα αμινοξέα.
3. Φωσφορυλίωση
Η φωσφορυλίωση είναι μια από τις πιο κοινές μετα-μεταφραστικές τροποποιήσεις στη φύση.Στα ανθρώπινα κύτταρα, περισσότερο από το 30% των πρωτεϊνών είναι φωσφορυλιωμένες.Η φωσφορυλίωση, ιδιαίτερα η αναστρέψιμη φωσφορυλίωση, παίζει σημαντικό ρόλο στον έλεγχο πολλών κυτταρικών διεργασιών, όπως η μεταγωγή σήματος, η έκφραση γονιδίων, η ρύθμιση του κυτταρικού κύκλου και του κυτταροσκελετού και η απόπτωση.
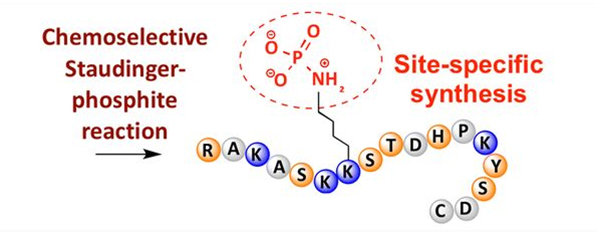
Η φωσφορυλίωση μπορεί να παρατηρηθεί σε μια ποικιλία υπολειμμάτων αμινοξέων, αλλά οι πιο συνηθισμένοι στόχοι φωσφορυλίωσης είναι τα υπολείμματα σερίνης, θρεονίνης και τυροσίνης.Τα παράγωγα φωσφοτυροσίνης, φωσφοθρεονίνης και φωσφοσερίνης μπορούν είτε να εισαχθούν στα πεπτίδια κατά τη διάρκεια της σύνθεσης είτε να σχηματιστούν μετά την πεπτιδική σύνθεση.Η επιλεκτική φωσφορυλίωση μπορεί να επιτευχθεί χρησιμοποιώντας υπολείμματα σερίνης, θρεονίνης και τυροσίνης που αφαιρούν επιλεκτικά τις προστατευτικές ομάδες.Ορισμένα αντιδραστήρια φωσφορυλίωσης μπορούν επίσης να εισάγουν ομάδες φωσφορικού οξέος στο πολυπεπτίδιο με μετατροποποίηση.Τα τελευταία χρόνια, η ειδική για τη θέση φωσφορυλίωση της λυσίνης έχει επιτευχθεί χρησιμοποιώντας μια χημικά εκλεκτική αντίδραση Staudinger-φωσφίτη (Εικόνα 3).
4. Μυριστουλίωση και παλμιτοϋλίωση
Η ακυλίωση του Ν-τερματικού άκρου με λιπαρά οξέα επιτρέπει στα πεπτίδια ή τις πρωτεΐνες να συνδέονται με τις κυτταρικές μεμβράνες.Η μυριδαμοϋλιωμένη αλληλουχία στο Ν-τερματικό άκρο επιτρέπει στις πρωτεϊνικές κινάσες της οικογένειας Src και στις πρωτεΐνες της αντίστροφης μεταγραφάσης Gaq να στοχευθούν για να συνδεθούν με τις κυτταρικές μεμβράνες.Το μυριστικό οξύ συνδέθηκε με το Ν-άκρο της ρητίνης-πολυπεπτιδίου χρησιμοποιώντας τυπικές αντιδράσεις σύζευξης και το προκύπτον λιποπεπτίδιο μπορούσε να διαχωριστεί υπό τυπικές συνθήκες και να καθαριστεί με RP-HPLC.
5. Γλυκοζυλίωση
Τα γλυκοπεπτίδια όπως η βανκομυκίνη και η τεικολανίνη είναι σημαντικά αντιβιοτικά για τη θεραπεία ανθεκτικών στα φάρμακα βακτηριακών λοιμώξεων και άλλα γλυκοπεπτίδια χρησιμοποιούνται συχνά για την τόνωση του ανοσοποιητικού συστήματος.Επιπλέον, δεδομένου ότι πολλά μικροβιακά αντιγόνα είναι γλυκοζυλιωμένα, είναι μεγάλης σημασίας να μελετηθούν τα γλυκοπεπτίδια για τη βελτίωση του θεραπευτικού αποτελέσματος της μόλυνσης.Από την άλλη πλευρά, έχει βρεθεί ότι οι πρωτεΐνες στην κυτταρική μεμβράνη των καρκινικών κυττάρων εμφανίζουν ανώμαλη γλυκοζυλίωση, η οποία κάνει τα γλυκοπεπτίδια να παίζουν σημαντικό ρόλο στην έρευνα για τον καρκίνο και την ανοσολογική άμυνα του όγκου.Τα γλυκοπεπτίδια παρασκευάζονται με τη μέθοδο Fmoc/t-Bu.Γλυκοζυλιωμένα υπολείμματα, όπως η θρεονίνη και η σερίνη, εισάγονται συχνά σε πολυπεπτίδια από fMOC που ενεργοποιούνται με πενταφθοροφαινολεστέρα για την προστασία των γλυκοζυλιωμένων αμινοξέων.
6. Ισοπρένιο
Η ισοπενταδιενυλίωση λαμβάνει χώρα σε υπολείμματα κυστεΐνης στην πλευρική αλυσίδα κοντά στο καρβοξυτελικό άκρο.Το ισοπρένιο πρωτεΐνης μπορεί να βελτιώσει τη συγγένεια της κυτταρικής μεμβράνης και να σχηματίσει αλληλεπίδραση πρωτεΐνης-πρωτεΐνης.Οι ισοπενταδιενωμένες πρωτεΐνες περιλαμβάνουν φωσφατάση τυροσίνης, μικρή GTase, μόρια κοχαπερόνης, πυρηνικό έλασμα και κεντρομερείς πρωτεΐνες δέσμευσης.Τα πολυπεπτίδια ισοπρενίου μπορούν να παρασκευαστούν χρησιμοποιώντας ισοπρένιο σε ρητίνες ή με την εισαγωγή παραγώγων κυστεΐνης.
7. Τροποποίηση πολυαιθυλενογλυκόλης (PEG).
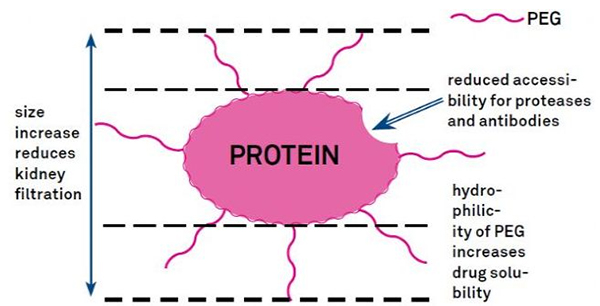
Η τροποποίηση PEG μπορεί να χρησιμοποιηθεί για τη βελτίωση της υδρολυτικής σταθερότητας της πρωτεΐνης, της βιοκατανομής και της διαλυτότητας των πεπτιδίων.Η εισαγωγή αλυσίδων PEG στα πεπτίδια μπορεί να βελτιώσει τις φαρμακολογικές τους ιδιότητες και επίσης να αναστείλει την υδρόλυση των πεπτιδίων από πρωτεολυτικά ένζυμα.Τα πεπτίδια PEG διέρχονται μέσω της σπειραματικής τριχοειδούς διατομής πιο εύκολα από τα συνηθισμένα πεπτίδια, μειώνοντας σημαντικά τη νεφρική κάθαρση.Λόγω του παρατεταμένου ενεργού χρόνου ημιζωής των πεπτιδίων PEG in vivo, το φυσιολογικό επίπεδο θεραπείας μπορεί να διατηρηθεί με χαμηλότερες δόσεις και λιγότερο συχνά πεπτιδικά φάρμακα.Ωστόσο, η τροποποίηση PEG έχει επίσης αρνητικά αποτελέσματα.Μεγάλες ποσότητες PEG εμποδίζουν το ένζυμο να αποικοδομήσει το πεπτίδιο και επίσης μειώνουν τη σύνδεση του πεπτιδίου στον υποδοχέα στόχο.Ωστόσο, η χαμηλή συγγένεια των πεπτιδίων PEG συνήθως αντισταθμίζεται από τη μεγαλύτερη φαρμακοκινητική ημιζωή τους και, καθώς υπάρχουν περισσότερο στο σώμα, τα πεπτίδια PEG έχουν μεγαλύτερη πιθανότητα να απορροφηθούν στους ιστούς στόχους.Επομένως, οι προδιαγραφές πολυμερούς PEG θα πρέπει να βελτιστοποιηθούν για βέλτιστα αποτελέσματα.Από την άλλη πλευρά, τα πεπτίδια PEG συσσωρεύονται στο ήπαρ λόγω μειωμένης νεφρικής κάθαρσης, με αποτέλεσμα μακρομοριακό σύνδρομο.Επομένως, οι τροποποιήσεις PEG πρέπει να σχεδιάζονται πιο προσεκτικά όταν χρησιμοποιούνται πεπτίδια για δοκιμές φαρμάκων.
Οι κοινές ομάδες τροποποίησης των τροποποιητών PEG μπορούν να συνοψιστούν χονδρικά ως εξής: Αμινο (-αμίνη) -NH2, αμινομεθυλ-Ch2-NH2, υδροξυ-ΟΗ, καρβοξυ-Cooh, σουλφυδρυλ (-Θειόλη) -SH, Μαλεϊμίδιο -MAL, ανθρακικό ηλεκτριμίδιο - SC, οξικό ηλεκτριμίδιο -SCM, προπιονικό ηλεκτριμίδιο -SPA, n-υδροξυηλεκτριμίδιο -NHS, ακρυλικό-ch2ch2cooh, αλδεΰδη -CHO (όπως propional-ald, butyrALD), ακρυλική βάση (-ακρυλικό-acrl), αζιδο-νυλαζίδιο, Βιοτίνη, φλουορεσκεΐνη, γλουταρυλ-GA, ακρυλικό υδραζίδιο, αλκυνο-αλκύνιο, π-τολουολοσουλφονικό -OTs, ηλεκτριμίδιο ηλεκτρικό -SS, κ.λπ. Τα παράγωγα PEG με καρβοξυλικά οξέα μπορούν να συζευχθούν με η-τελικές αμίνες ή πλευρικές αλυσίδες λυσίνης.Το αμινο-ενεργοποιημένο PEG μπορεί να συζευχθεί με πλευρικές αλυσίδες ασπαρτικού οξέος ή γλουταμικού οξέος.Η κακώς ενεργοποιημένη PEG μπορεί να συζευχθεί με τη μερκαπτάνη πλήρως αποπροστατευμένων πλευρικών αλυσίδων κυστεΐνης [11].Οι τροποποιητές PEG ταξινομούνται συνήθως ως εξής (σημείωση: το mPEG είναι μεθοξυ-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) τροποποιητής PEG ευθείας αλυσίδας
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2) διλειτουργικός τροποποιητής PEG
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) διακλαδούμενος τροποποιητής PEG
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Βιοτινοποίηση
Η βιοτίνη μπορεί να συνδεθεί ισχυρά με την αβιδίνη ή τη στρεπταβιδίνη και η ισχύς δέσμευσης πλησιάζει ακόμη και τον ομοιοπολικό δεσμό.Τα επισημασμένα με βιοτίνη πεπτίδια χρησιμοποιούνται συνήθως σε ανοσοπροσδιορισμό, ιστοκυτταροχημεία και κυτταρομετρία ροής με βάση τον φθορισμό.Επισημασμένα αντισώματα αντιβιοτίνης μπορούν επίσης να χρησιμοποιηθούν για τη σύνδεση βιοτινυλιωμένων πεπτιδίων.Οι ετικέτες βιοτίνης είναι συχνά προσαρτημένες στην πλευρική αλυσίδα της λυσίνης ή στο Ν τερματικό.Το 6-αμινοκαπροϊκό οξύ χρησιμοποιείται συχνά ως δεσμός μεταξύ πεπτιδίων και βιοτίνης.Ο δεσμός είναι εύκαμπτος στη σύνδεση με το υπόστρωμα και συνδέεται καλύτερα με την παρουσία στερεοχημικής παρεμπόδισης.
9. Φθορίζουσα επισήμανση
Η σήμανση με φθορισμό μπορεί να χρησιμοποιηθεί για τον εντοπισμό πολυπεπτιδίων σε ζωντανά κύτταρα και για τη μελέτη ενζύμων και μηχανισμών δράσης.Η τρυπτοφάνη (Trp) είναι φθορίζουσα, επομένως μπορεί να χρησιμοποιηθεί για ενδογενή επισήμανση.Το φάσμα εκπομπής της τρυπτοφάνης εξαρτάται από το περιφερειακό περιβάλλον και μειώνεται με τη μείωση της πολικότητας του διαλύτη, μια ιδιότητα που είναι χρήσιμη για την ανίχνευση της δομής του πεπτιδίου και της δέσμευσης του υποδοχέα.Ο φθορισμός της τρυπτοφάνης μπορεί να σβήσει με πρωτονιωμένο ασπαρτικό οξύ και γλουταμικό οξύ, τα οποία μπορεί να περιορίσουν τη χρήση του.Η ομάδα χλωριούχου Dansyl (Dansyl) είναι πολύ φθορίζουσα όταν συνδέεται με μια αμινομάδα και χρησιμοποιείται συχνά ως φθορίζουσα ετικέτα για αμινοξέα ή πρωτεΐνες.
Συντονισμός φθορισμού Η μετατροπή ενέργειας (FRET) είναι χρήσιμη για μελέτες ενζύμων.Όταν εφαρμόζεται FRET, το πολυπεπτίδιο υποστρώματος συνήθως περιέχει μια ομάδα σήμανσης φθορισμού και μια ομάδα απόσβεσης φθορισμού.Οι επισημασμένες φθορίζουσες ομάδες σβήνονται από τον αποσβεστήρα μέσω μεταφοράς ενέργειας χωρίς φωτόνιο.Όταν το πεπτίδιο διαχωρίζεται από το εν λόγω ένζυμο, η ομάδα σήμανσης εκπέμπει φθορισμό.
10. Πολυπεπτίδια κλωβού
Τα πεπτίδια κλωβού έχουν οπτικά αφαιρούμενες προστατευτικές ομάδες που προστατεύουν το πεπτίδιο από τη σύνδεση με τον υποδοχέα.Όταν εκτίθεται σε υπεριώδη ακτινοβολία, το πεπτίδιο ενεργοποιείται, αποκαθιστώντας τη συγγένειά του με τον υποδοχέα.Επειδή αυτή η οπτική ενεργοποίηση μπορεί να ελεγχθεί ανάλογα με το χρόνο, το πλάτος ή την τοποθεσία, τα πεπτίδια κλωβού μπορούν να χρησιμοποιηθούν για τη μελέτη αντιδράσεων που συμβαίνουν στα κύτταρα.Οι πιο συχνά χρησιμοποιούμενες προστατευτικές ομάδες για πολυπεπτίδια κλωβού είναι οι 2-νιτροβενζυλικές ομάδες και τα παράγωγά τους, τα οποία μπορούν να εισαχθούν στη σύνθεση πεπτιδίων μέσω προστατευτικών παραγώγων αμινοξέων.Τα παράγωγα αμινοξέων που έχουν αναπτυχθεί είναι η λυσίνη, η κυστεΐνη, η σερίνη και η τυροσίνη.Τα ασπαρτικά και τα γλουταμικά παράγωγα, ωστόσο, δεν χρησιμοποιούνται συνήθως λόγω της ευαισθησίας τους σε κυκλοποίηση κατά τη σύνθεση και διάσπαση πεπτιδίων.
11. Πολυαντιγονικό πεπτίδιο (MAP)
Τα βραχέα πεπτίδια συνήθως δεν είναι άνοσα και πρέπει να συζευχθούν με πρωτεΐνες φορείς για την παραγωγή αντισωμάτων.Το πολυαντιγονικό πεπτίδιο (MAP) αποτελείται από πολλαπλά πανομοιότυπα πεπτίδια συνδεδεμένα με πυρήνες λυσίνης, τα οποία μπορούν να εκφράζουν ειδικά ανοσογόνα υψηλής ισχύος και μπορούν να χρησιμοποιηθούν για την παρασκευή δίστιχων πρωτεΐνης φορέα πεπτιδίου.Τα πολυπεπτίδια ΜΑΡ μπορούν να συντεθούν με σύνθεση στερεάς φάσης σε ρητίνη ΜΑΡ.Ωστόσο, η ατελής σύζευξη οδηγεί σε ελλείψεις ή κολοβωμένες πεπτιδικές αλυσίδες σε ορισμένους κλάδους και έτσι δεν εμφανίζει τις ιδιότητες του αρχικού πολυπεπτιδίου MAP.Ως εναλλακτική λύση, τα πεπτίδια μπορούν να παρασκευαστούν και να καθαριστούν χωριστά και στη συνέχεια να συζευχθούν με ΜΑΡ.Η πεπτιδική αλληλουχία που συνδέεται με τον πυρήνα του πεπτιδίου είναι καλά καθορισμένη και χαρακτηρίζεται εύκολα με φασματομετρία μάζας.
συμπέρασμα
Η τροποποίηση πεπτιδίων είναι ένα σημαντικό μέσο σχεδιασμού πεπτιδίων.Τα χημικά τροποποιημένα πεπτίδια μπορούν όχι μόνο να διατηρήσουν υψηλή βιολογική δραστηριότητα, αλλά επίσης να αποφύγουν αποτελεσματικά τα μειονεκτήματα της ανοσογονικότητας και της τοξικότητας.Ταυτόχρονα, η χημική τροποποίηση μπορεί να προσδώσει στα πεπτίδια μερικές νέες εξαιρετικές ιδιότητες.Τα τελευταία χρόνια, η μέθοδος ενεργοποίησης CH για την μετατροποποίηση πολυπεπτιδίων έχει αναπτυχθεί γρήγορα και έχουν επιτευχθεί πολλά σημαντικά αποτελέσματα.
Ώρα δημοσίευσης: Μαρ-20-2023
